製品情報
-

内視鏡システム
-
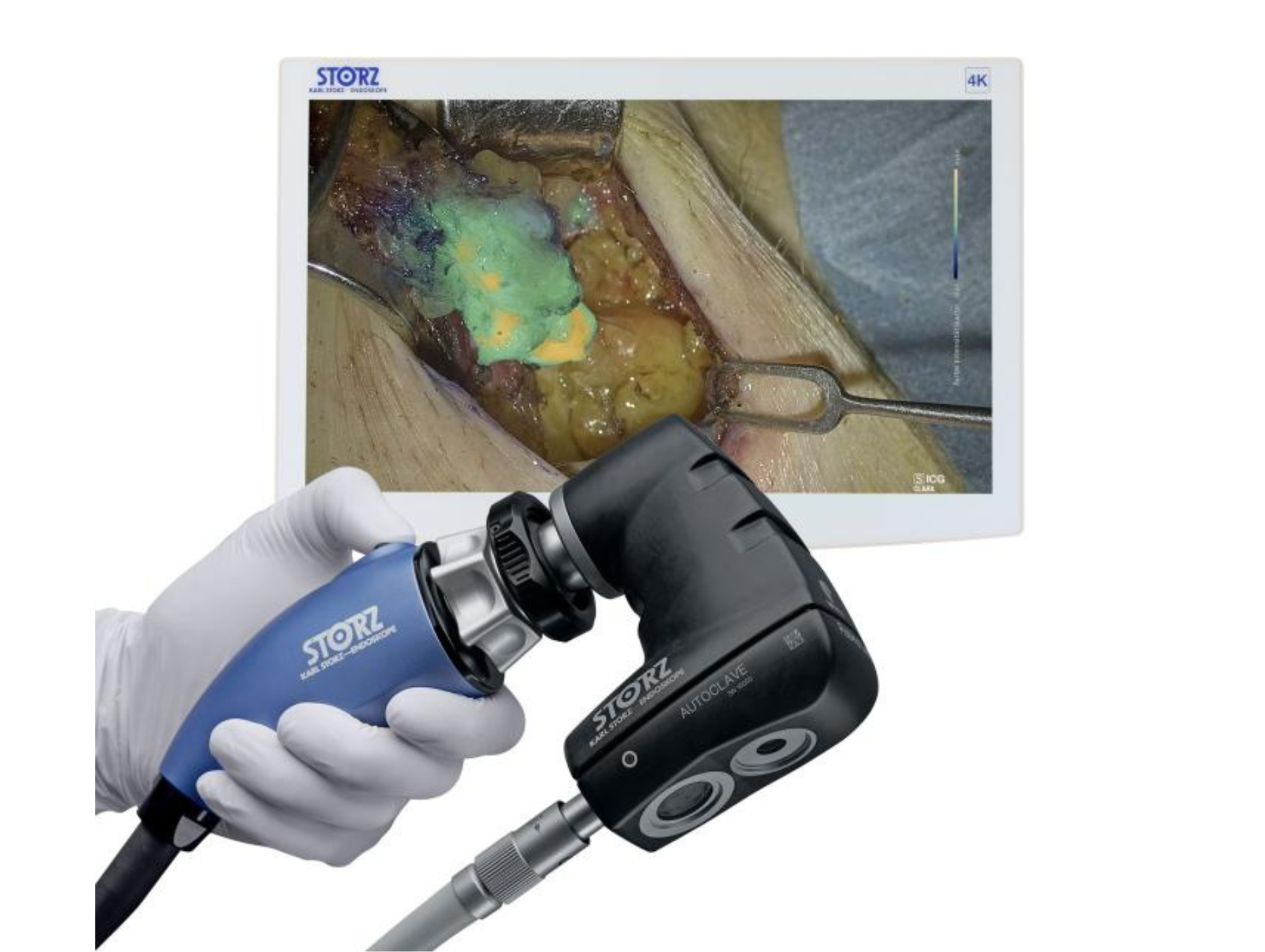
外視鏡
-

内視鏡手術用関連製品
-
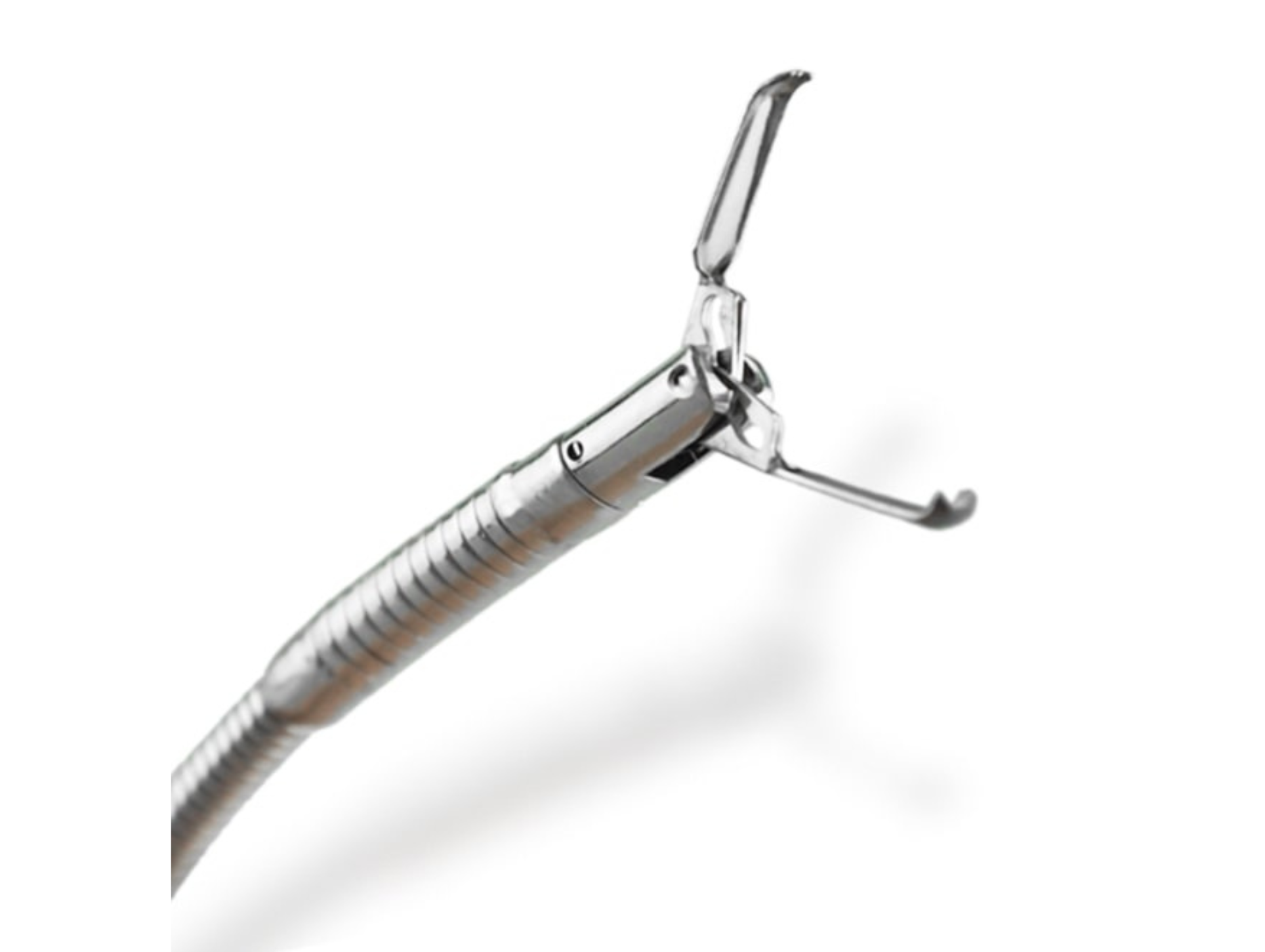
消化器内科関連
-

電気メス本体
-
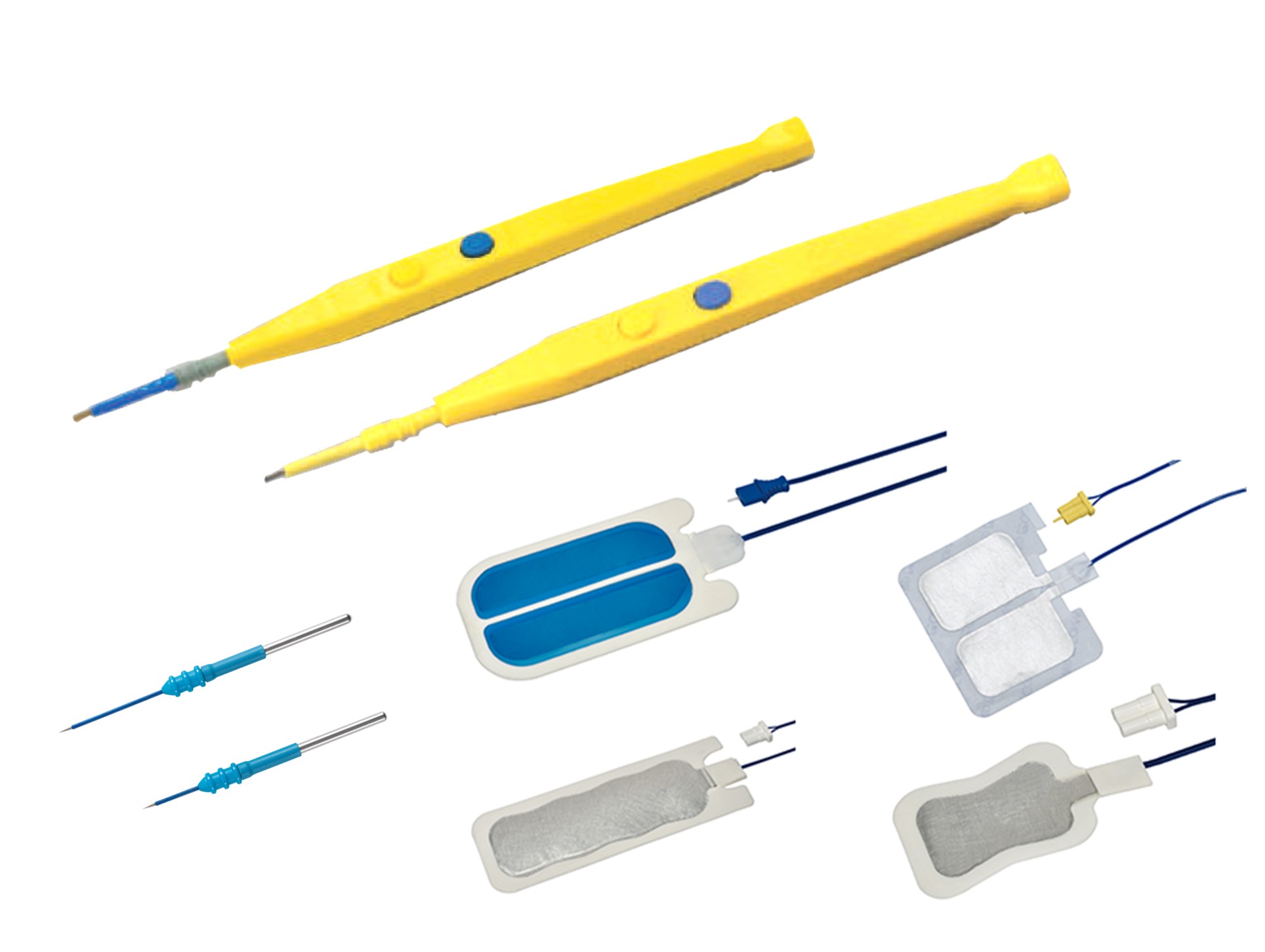
電気メスアクセサリー
-
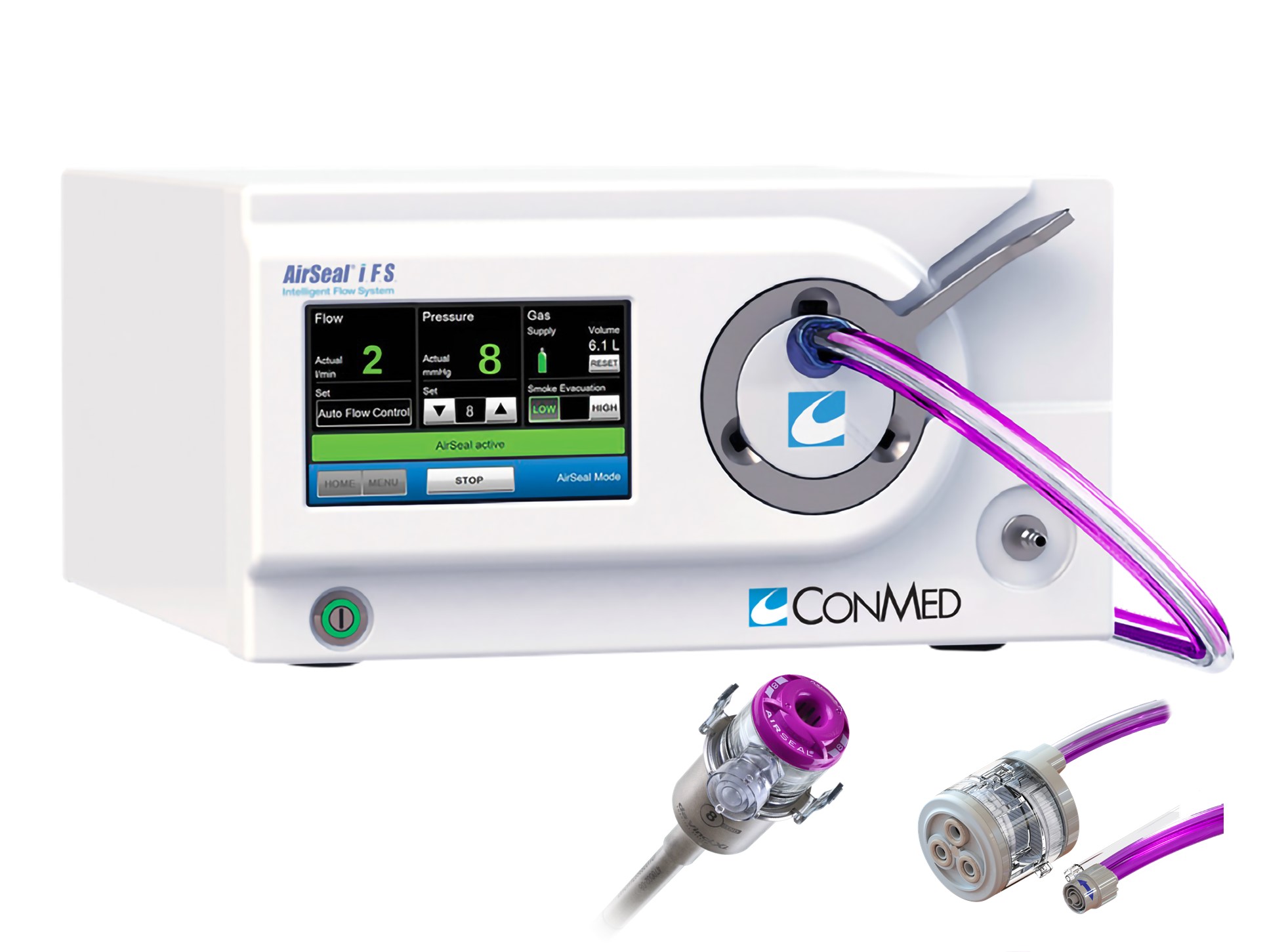
気腹装置
-
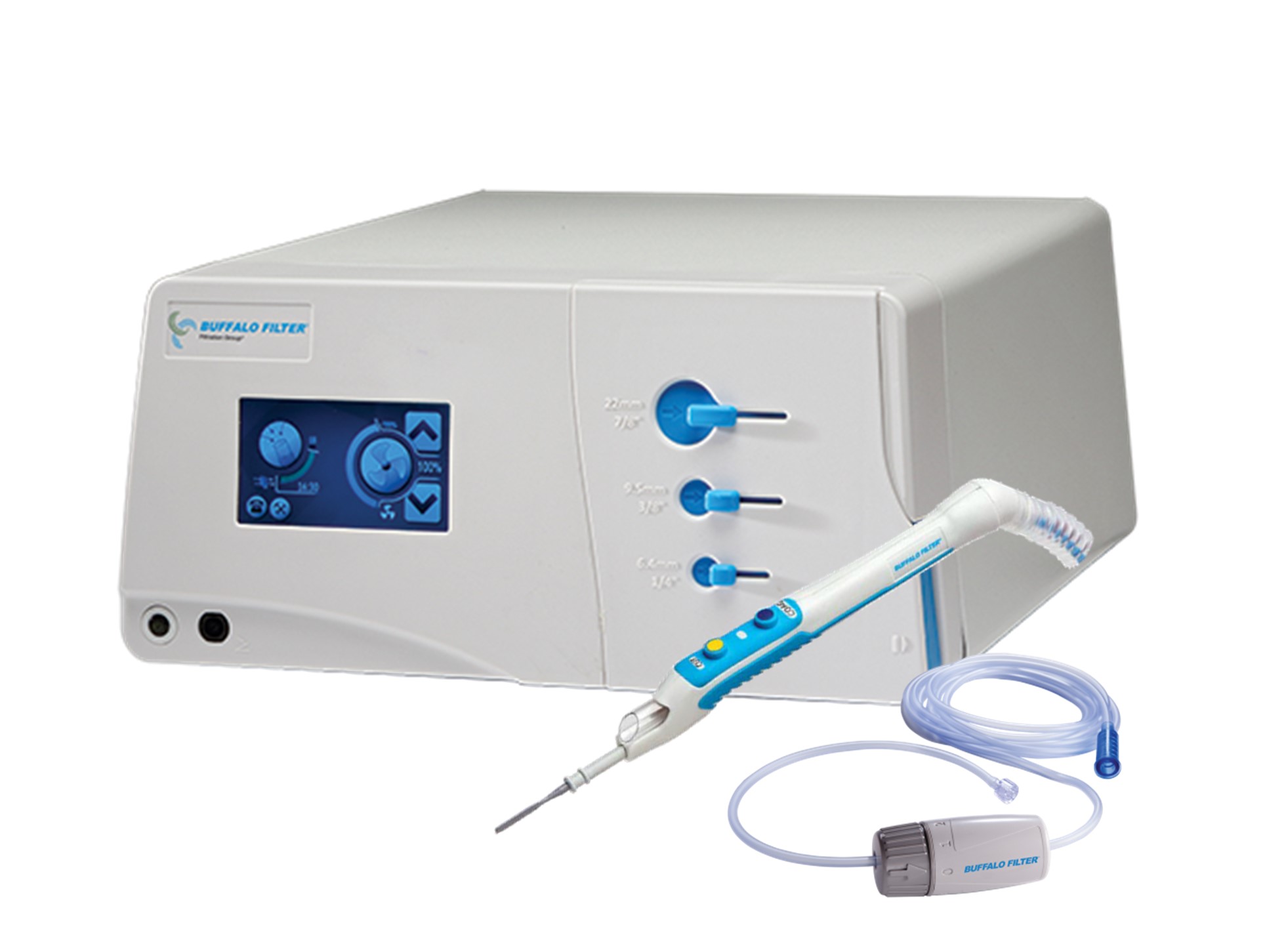
排煙システム
-
生検針
-

吸収性縫合糸
-

スコープマネジメント器具
-

尿管鏡
-
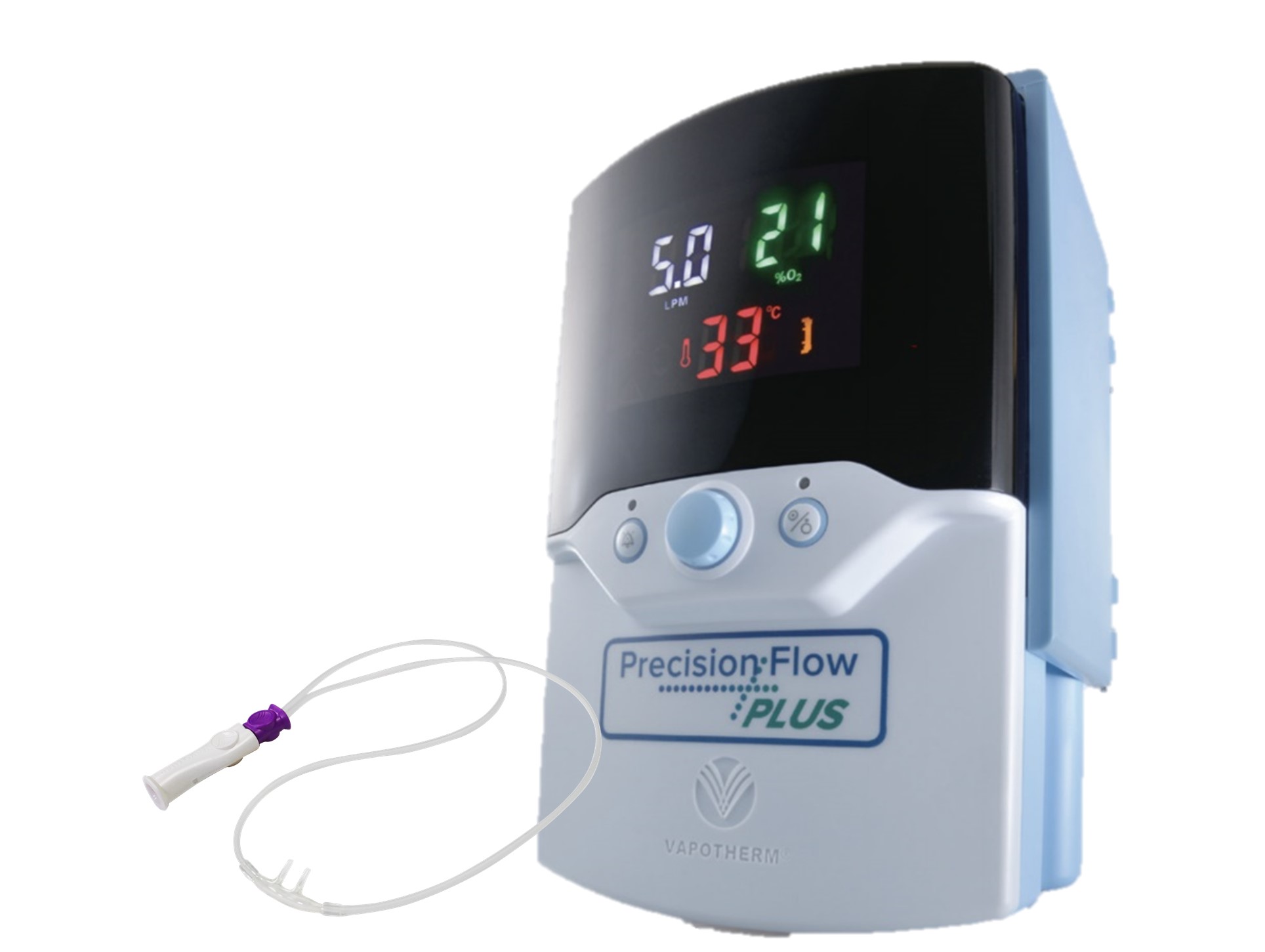
ハイフローネーザルカニューラシステム
-

脊椎製品
-

酸素療法アクセサリー/呼吸訓練器具
-
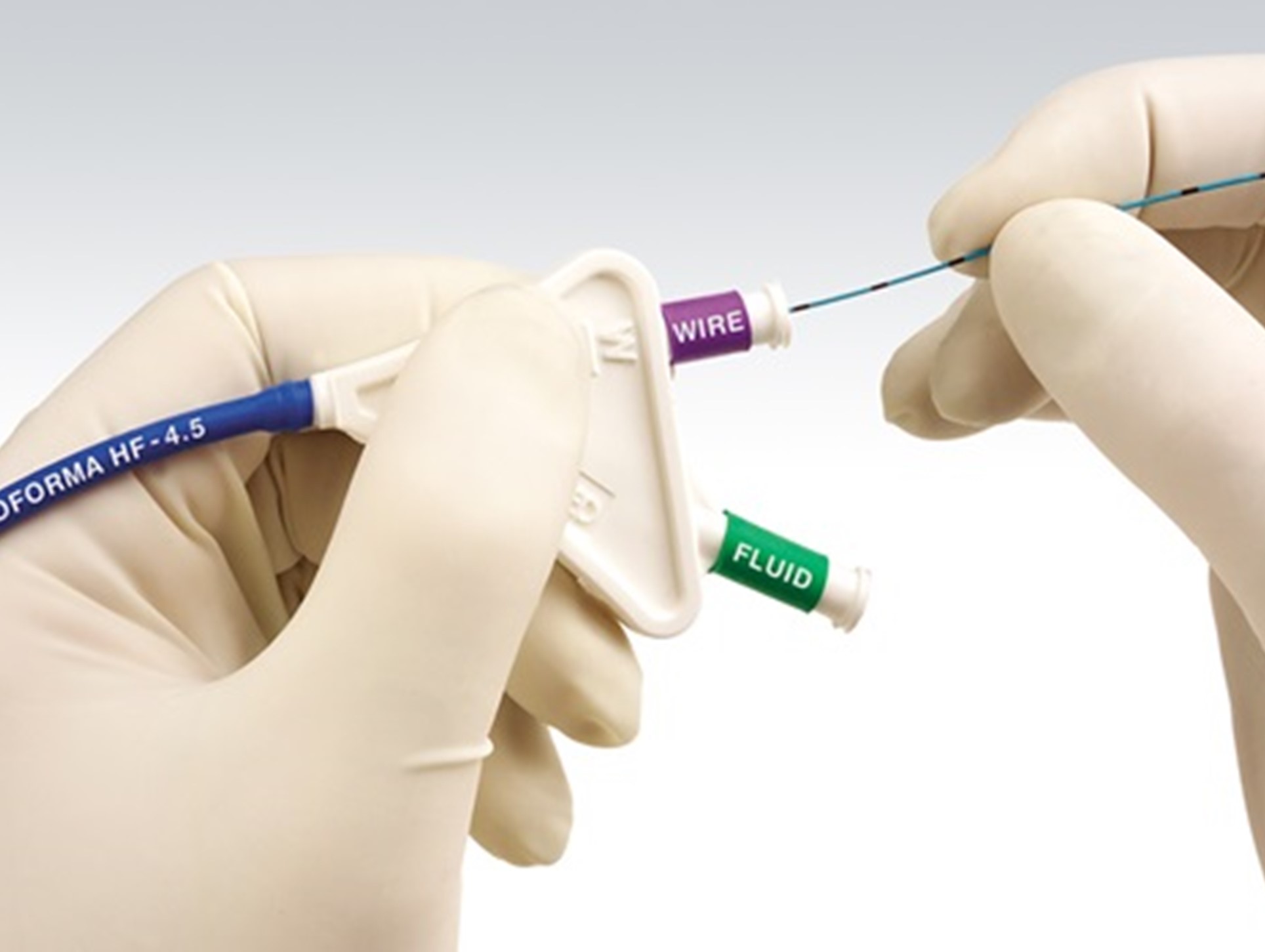
内視鏡処置具
-
吸収性骨再生用材料
-
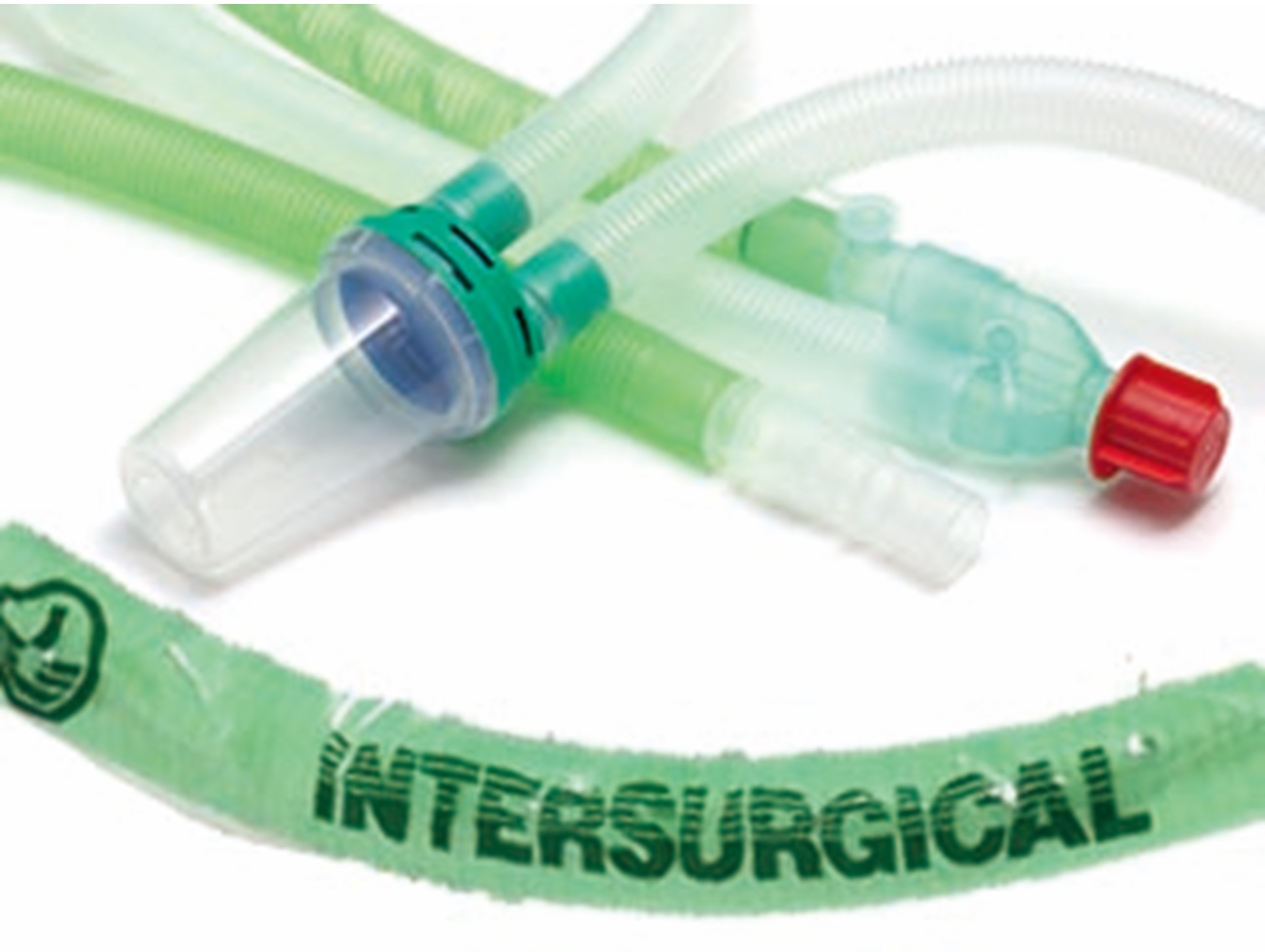
人工呼吸器周辺アクセサリー
-
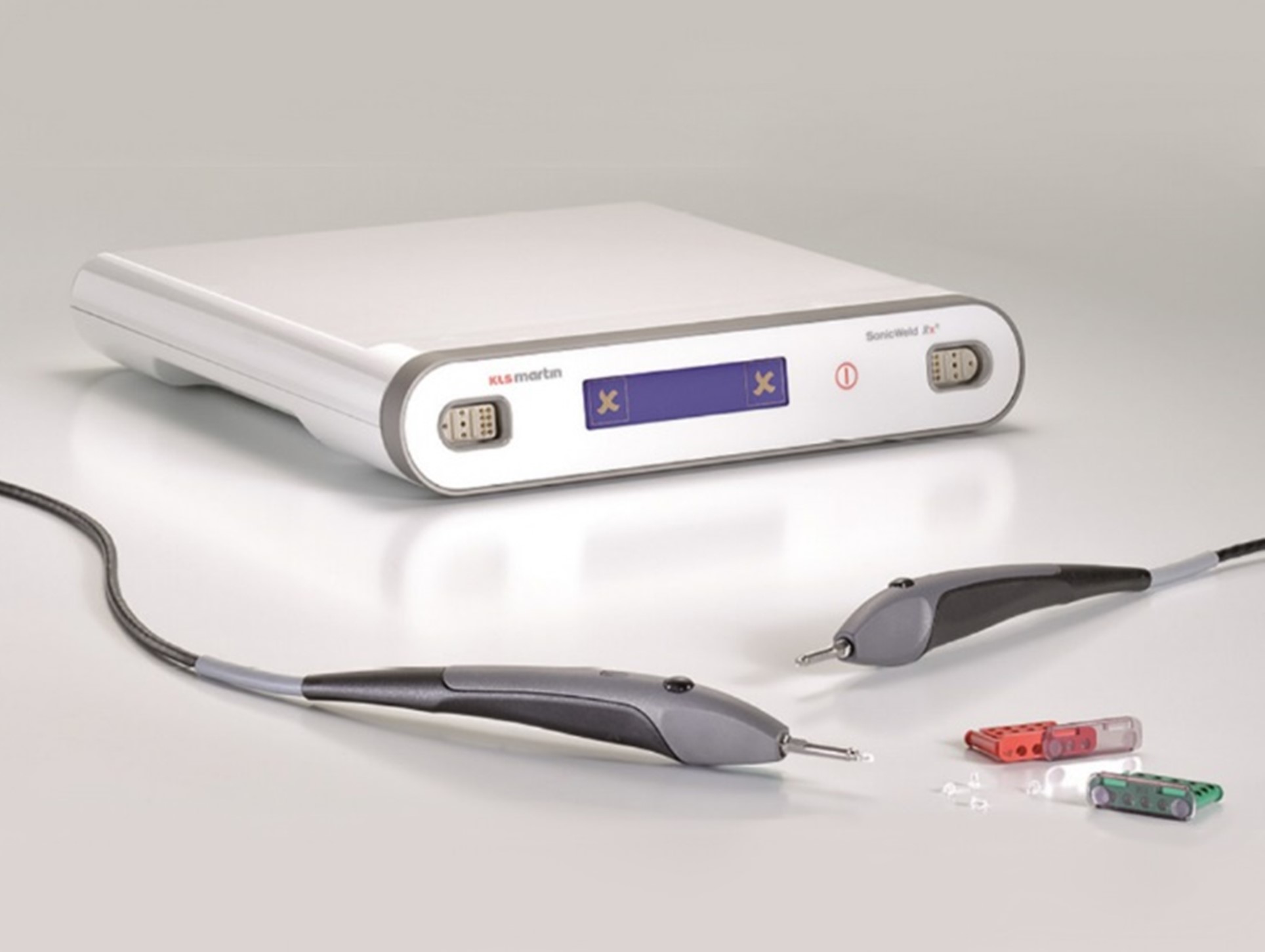
CMFインプラント
-

整形外科用ドリル
-

骨接合材料(内固定)
-

人工関節製品
-
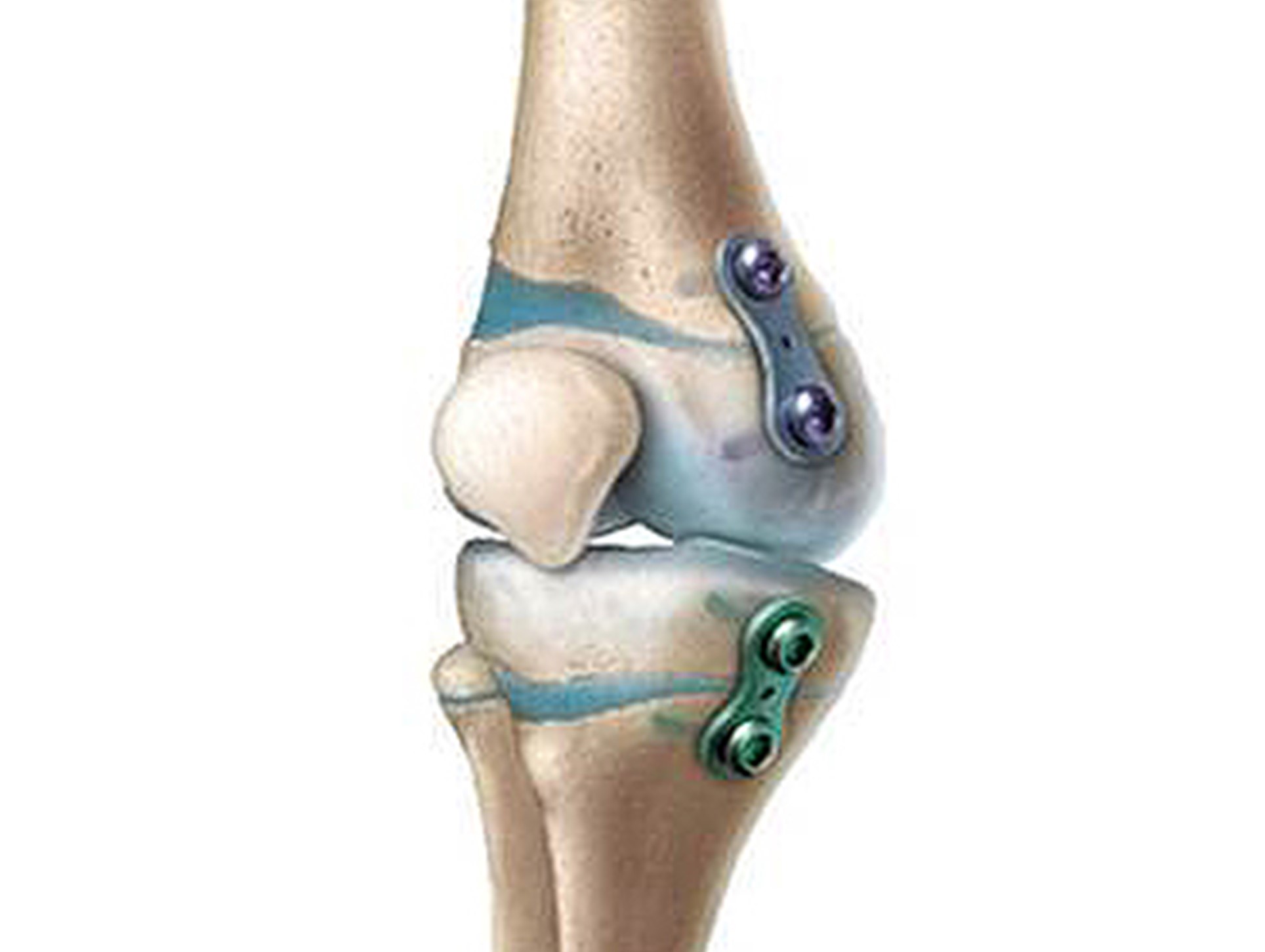
The Guided Growth System
-

創外固定器
-

パワーツールシステム
-
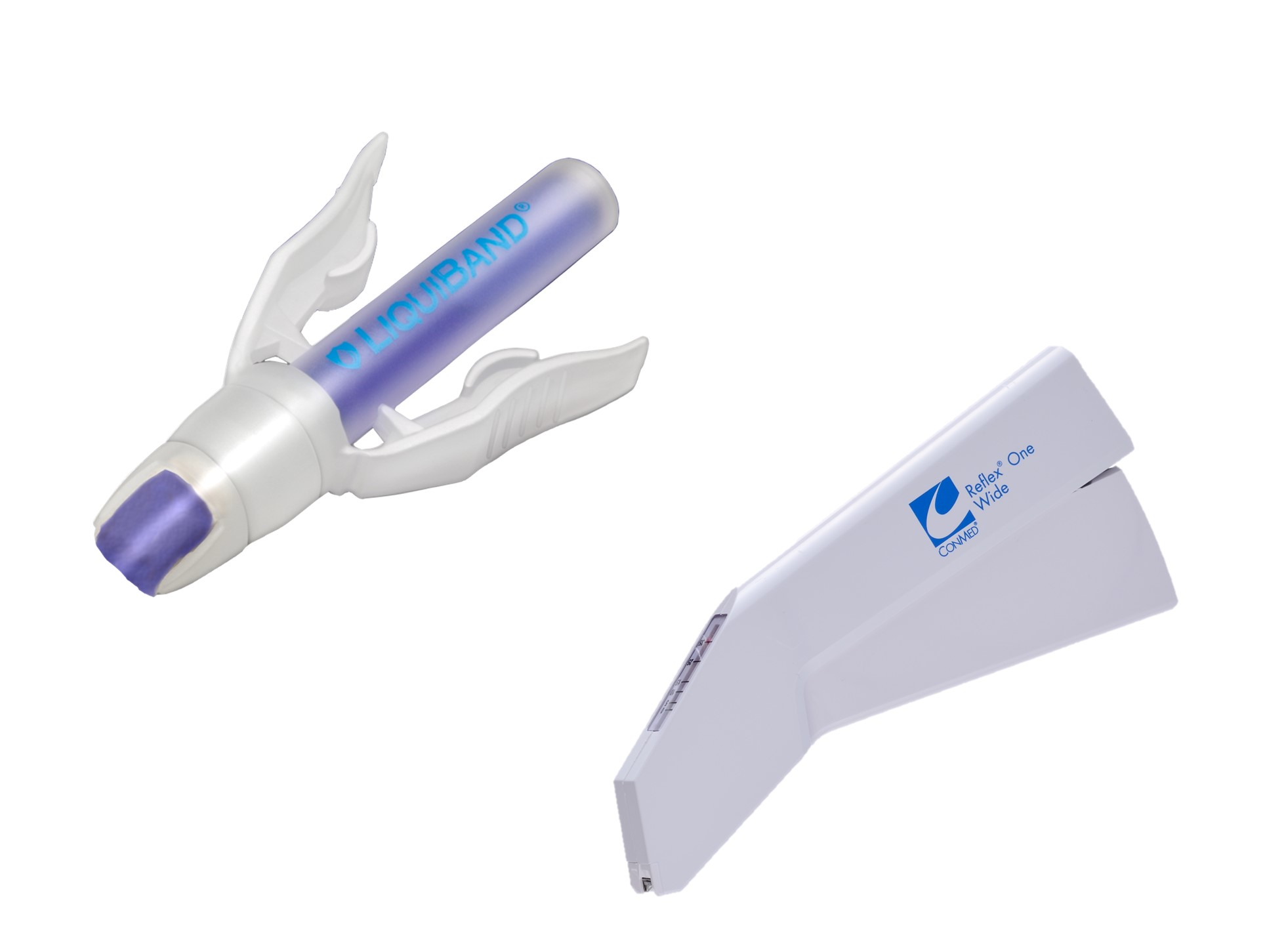
皮膚用接着剤 / スキンステープラー
-
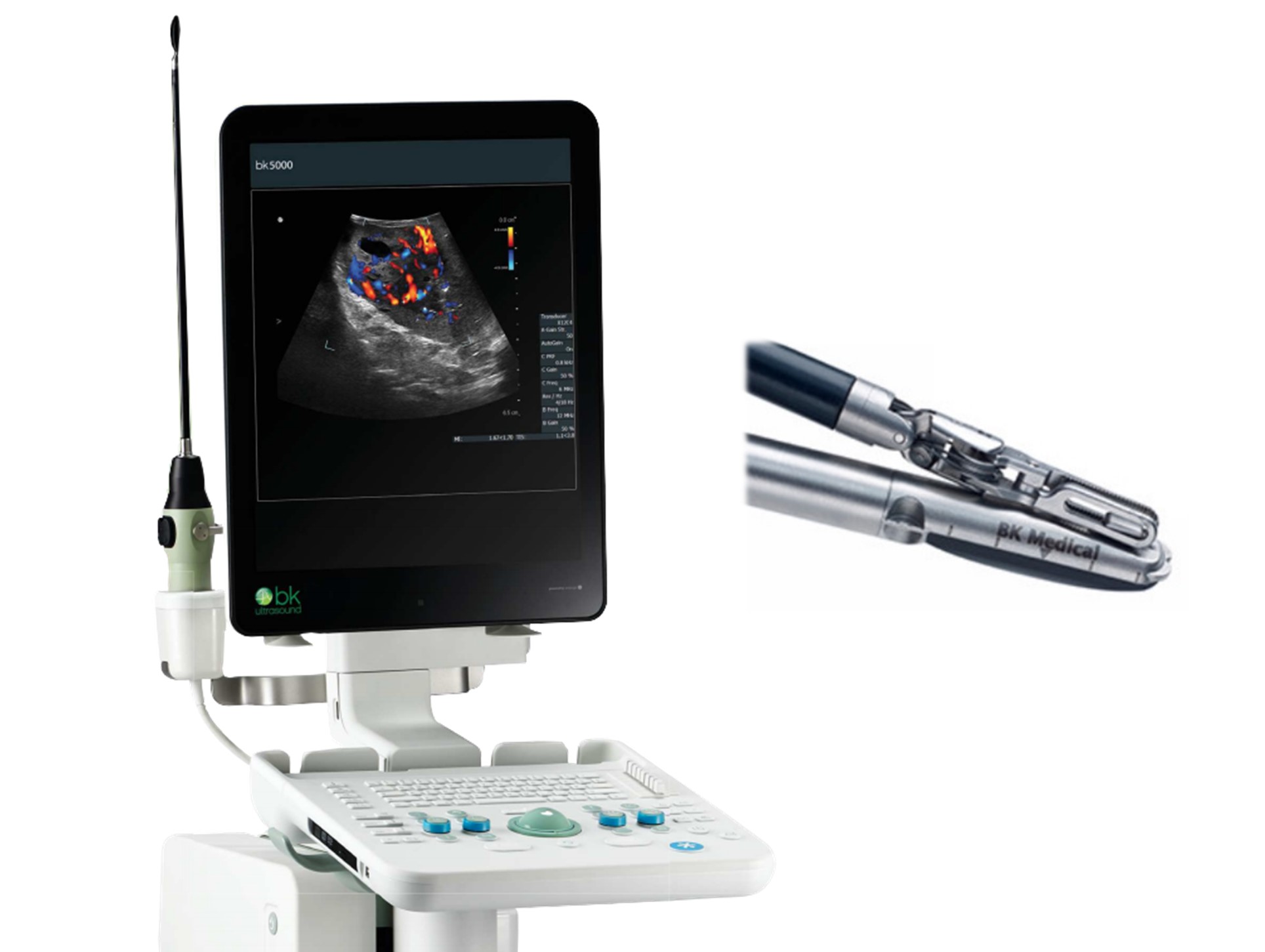
超音波診断装置(外科泌尿器用)
-

プローブカバー
-
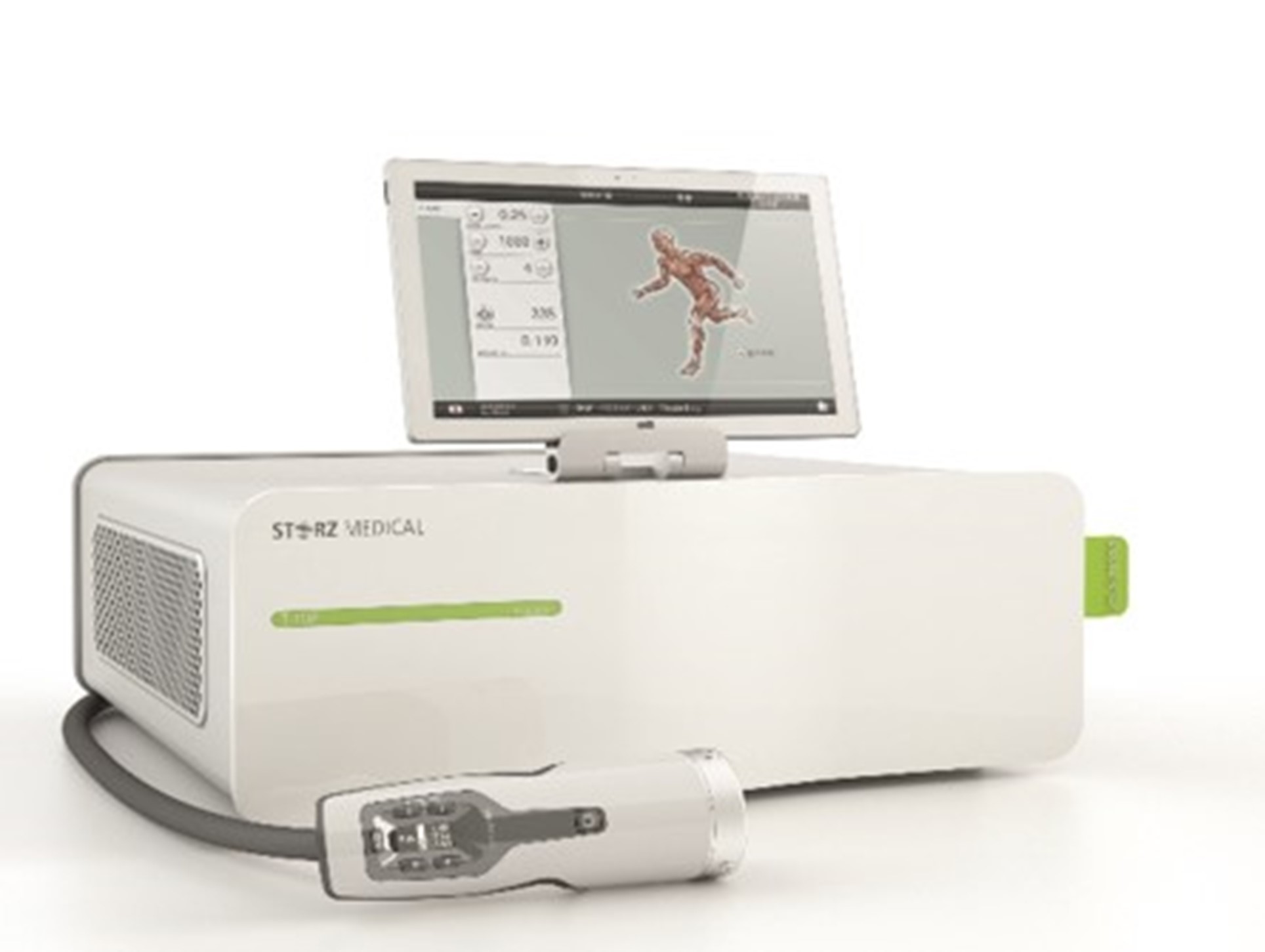
体外衝撃波疼痛治療器
-

超音波吸引器
-
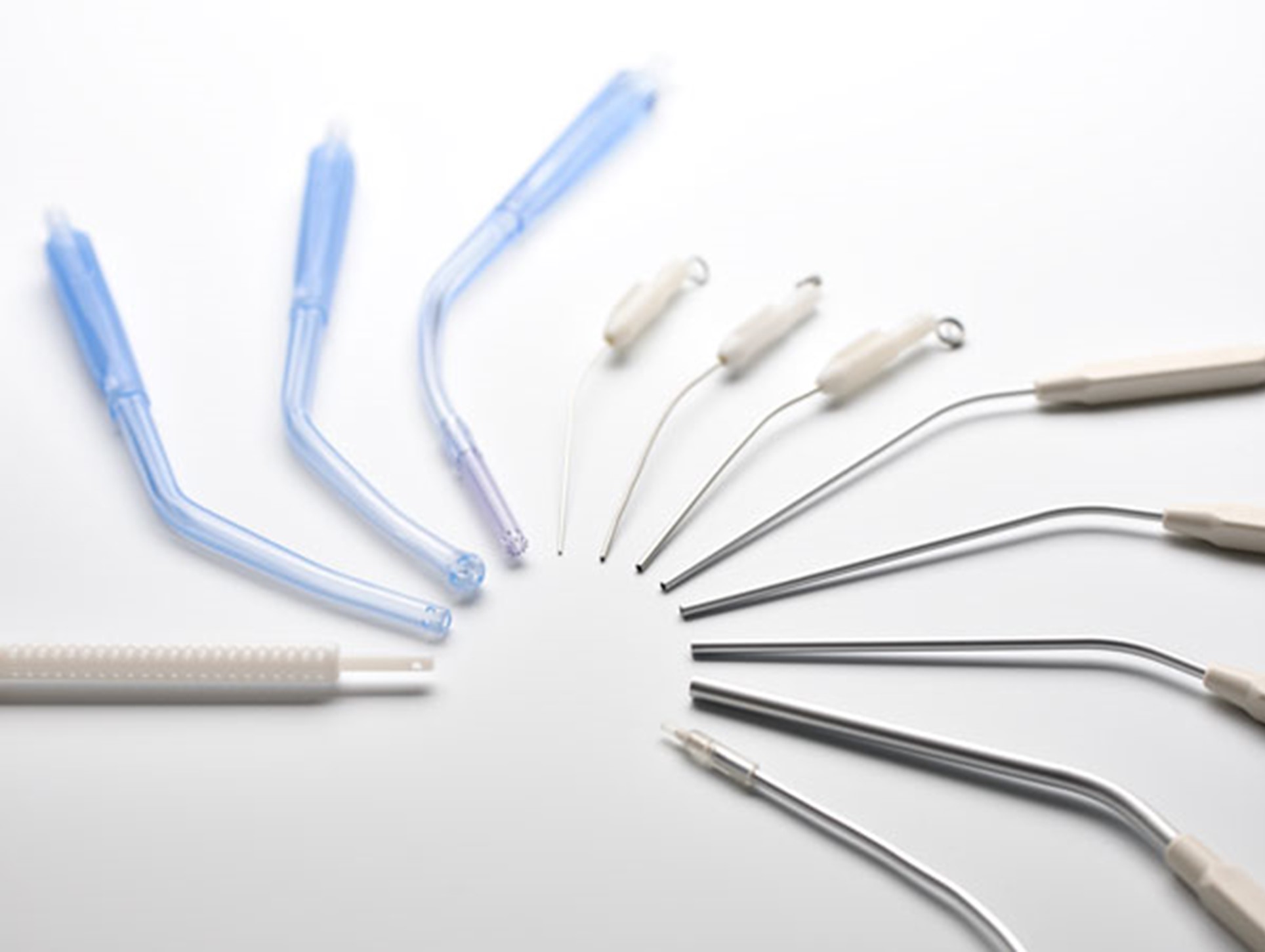
吸引関連製品
-

麻酔・蘇生関連器具
-
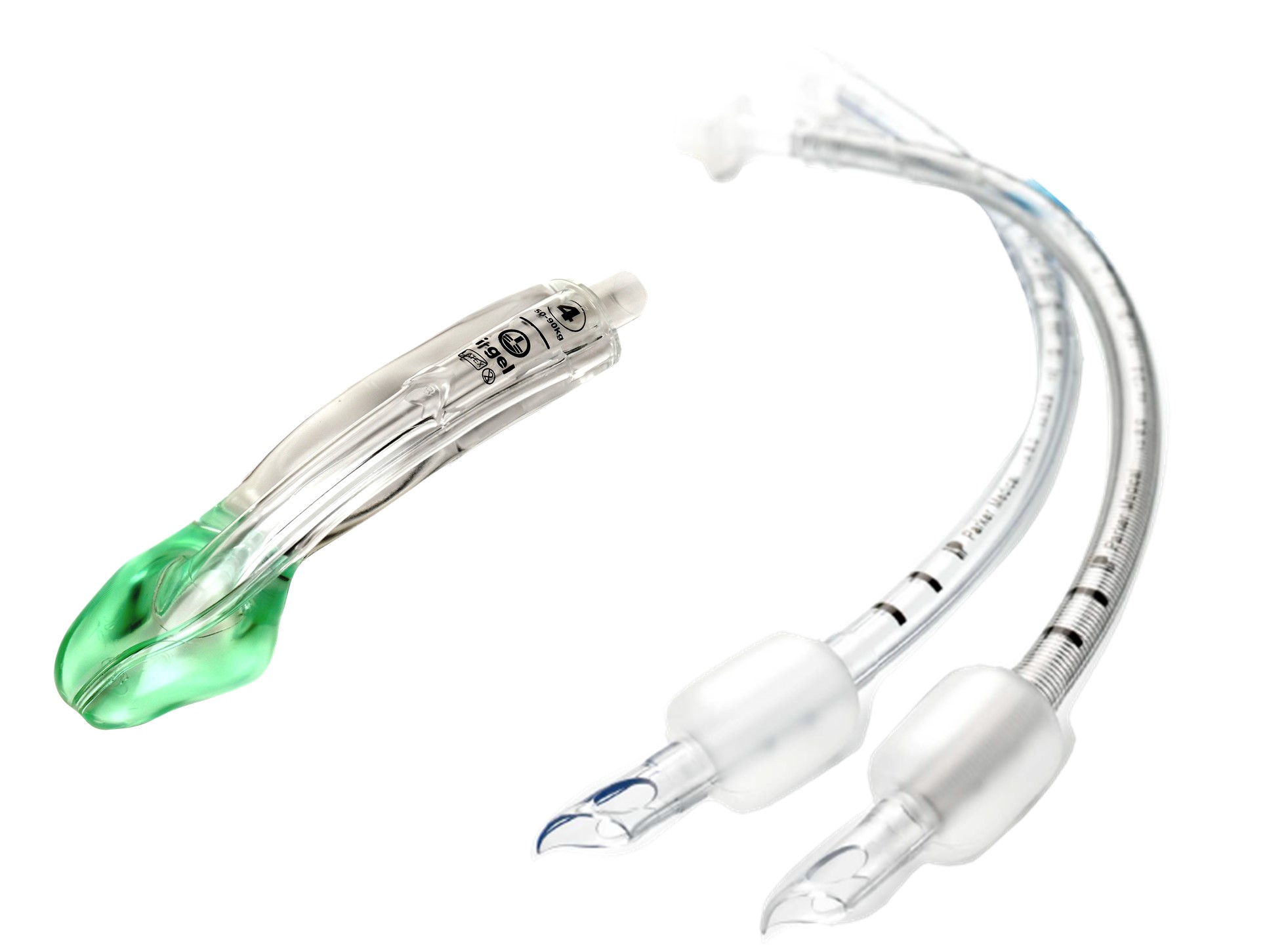
気管チューブ/声門上器具
-

血栓予防用弾性ストッキング
-
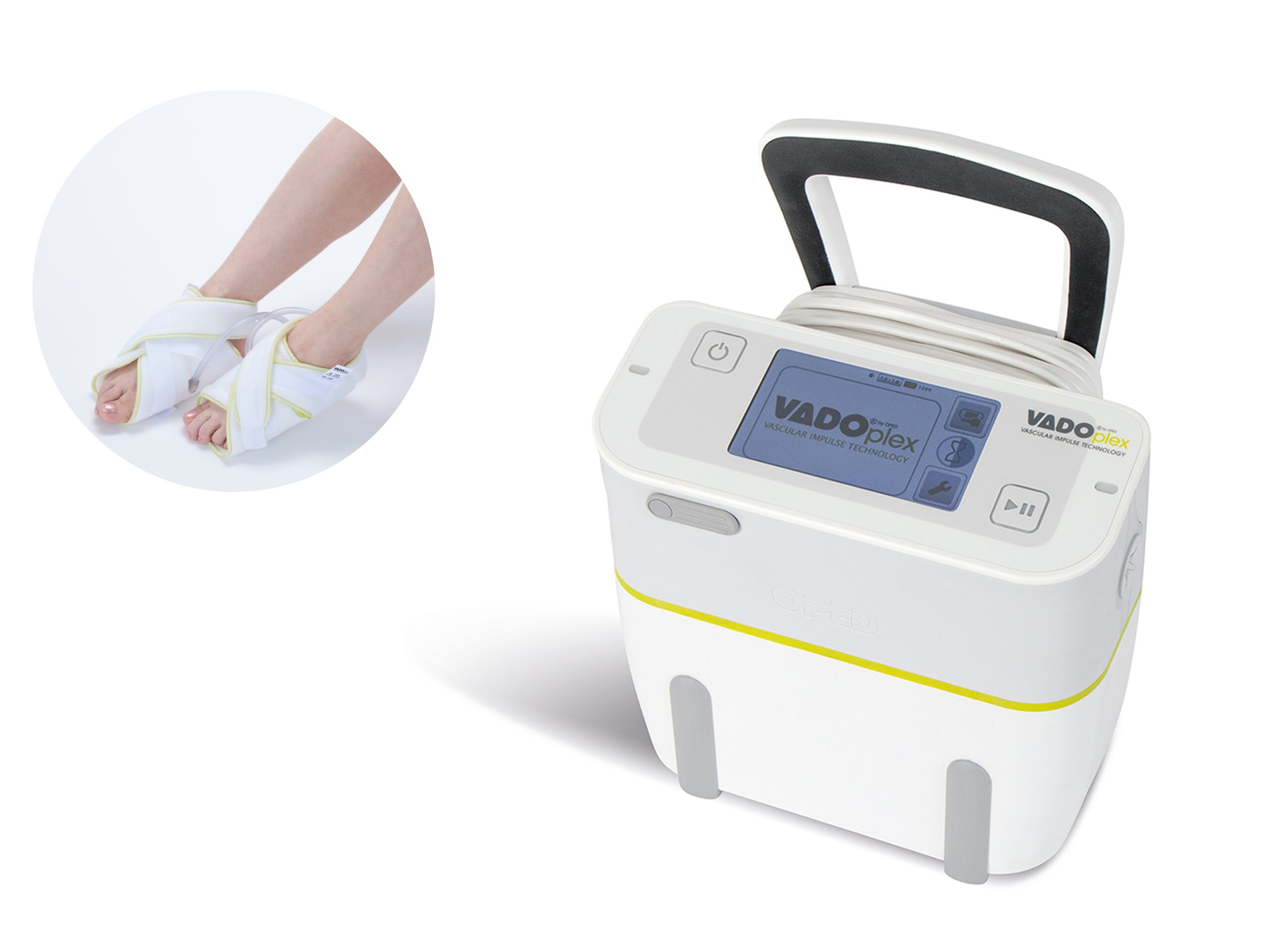
DVT予防用フットポンプ
-
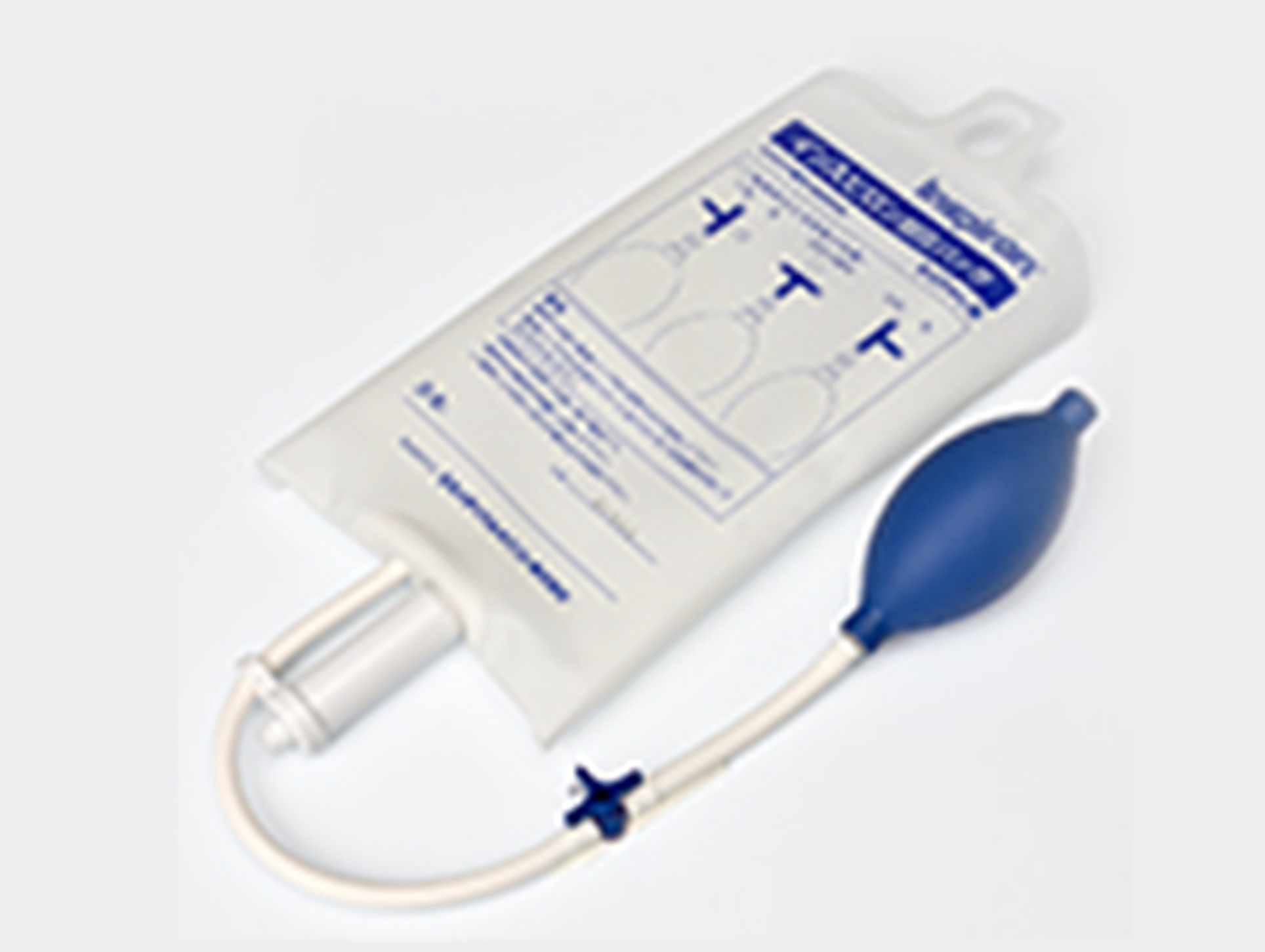
加圧バッグ
-
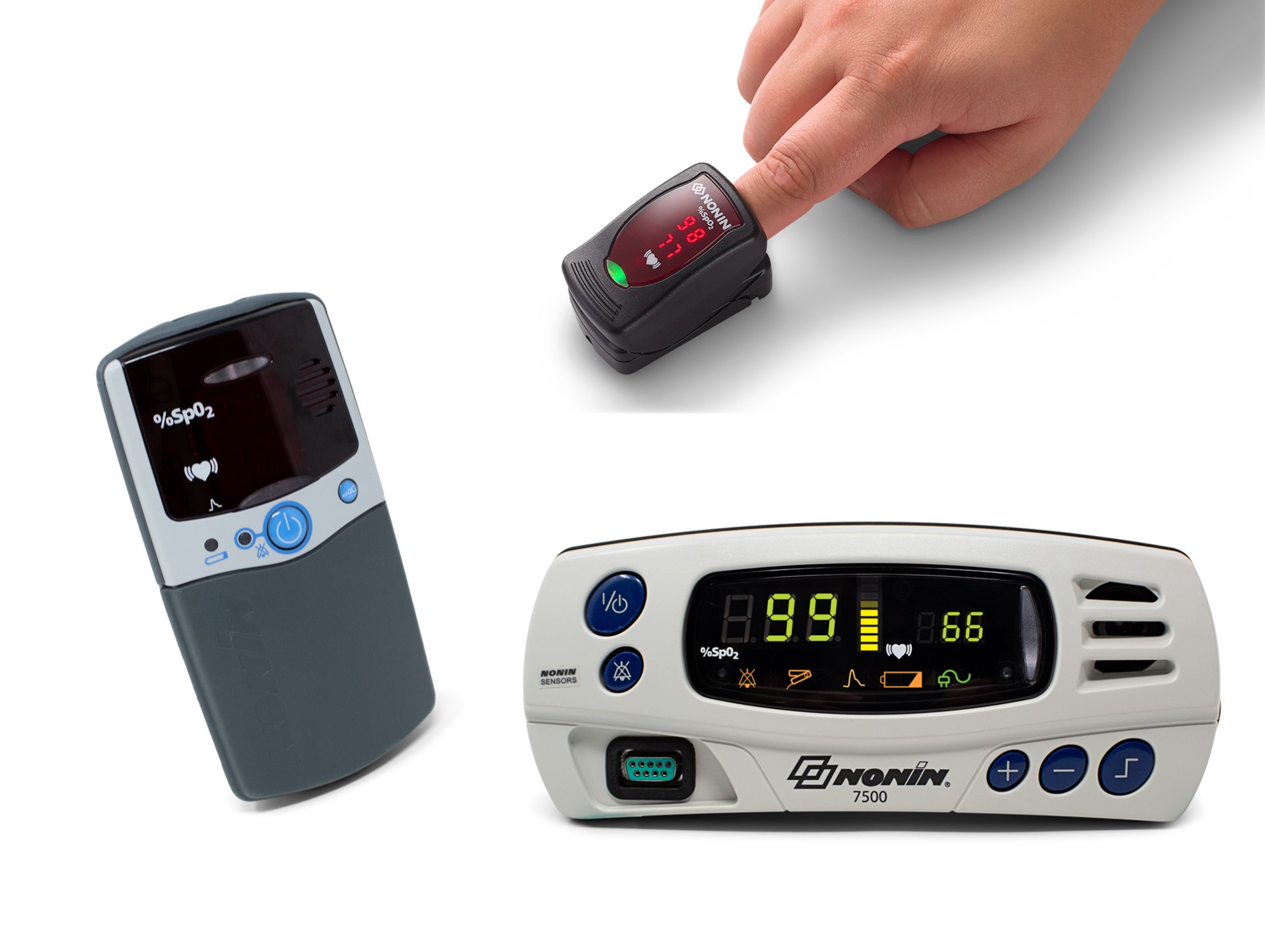
パルスオキシメトリー
-

ECG電極
-

インフューザー
-

産科関連
-

頭蓋骨穿孔用パーフォレーター/頭皮クリップ
-

定位放射線治療装置
-

トレーニングボックス
各種お問い合わせ
ご案内
- トップ
- ご案内
当サイトは医家向け情報を含んでおります。医家向け情報の公開は薬機法上、医療従事者に限定されています。
ご希望されたページは医療関係のお客様への情報提供を目的としており、一般の方や患者様への情報提供を目的としたものではございませんので、何卒ご理解下さいますようお願いいたします。
あなたは医療従事者ですか?
総合お問い合わせはこちらから